ͼ10. ͼƬ����Cell, doi:10.1016/j.cell.2018.04.005��
2018��4�£�Malcolm A. Martin�Ŷ��ڸ�����ǿ������HIV�����кͿ����������ͻ����о���Ա�Ʊ������ֱַ����3BNC117-LS��10-1074-LS�ľ���ע���Ϳ��塣����ע��ÿ�ֿ��嶼�����ڳ���37�ܵ�ʱ���ﱣ��2�飨ÿ��6ֻ��ÿ�ܱ�¶��Գ-��������ȱ�ݲ�����SHIV���ĺ������ܸ�Ⱦ���������ܿ������Ƶĺ������ܺ��ȾHIV[22]��
2018��3�£�Guochun Jiang�����״μ�����øACSS2�������鵰�װͶ��������ο���תHIVDZ�����ٽ����ֲ�������ת¼[23]����Ҳ�����鵰��ȥ�Ͷ�����Ҳ��HIVDZ���ı����Ŵ���־���������鵰�İͶ��������λ������뿹HIVDZ����ҩ����絰��øC������PEP005��HDAC���Ƽ�����ŵ����һ��Эͬ����������HIV�ĸ�Ⱦ��
2018��2�£�Ryan P. McNamara���˷��ַ���HIV����ʹ�������彫��������Nef���ڵ�ϸ����[24]��������Ϊ����������Nef���������ֲ����ӿ�AIDS��չ�Ļ���֮һ��
2018��2�£�Xilin Wu���˿�����һ�����͵ĵ��������Ĵ��������к��Կ��壬��Ϊ��BiIA-SG�������ܹ�ʵ��һʯ�����Ŀ�ģ�ͨ����ϵ���������CD4�ϣ�BiIA-SG���ܴ�ս���Ϲ�����������ϸ����HIV-1�Ӷ�����CD4+ Tϸ�����ܸ�Ⱦ������������ܹ���Ч����124���Ŵ������Ե�HIV-1���꣬���ܹ���Ч�������ֲ�������Դ��С�����ڵĻ���[25]��BiIA-SG������Ϊһ������ͨ���͵Ŀ���ҩ������ЧԤ��HIV-1�ĸ�Ⱦ��
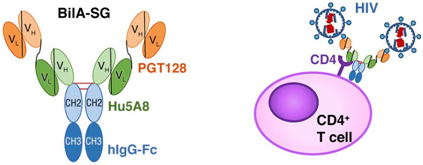
ͼ11. BiIA-SGʾ��ͼ��ͼƬ����Journal of Clinical Investigation, doi:10.1172/JCI96764��
2018��1�£�Szu-Han Huang���˷���DZ����HIV�����⣨latent HIV reservoir����CD8+ Tϸ�����ֳ��ֿ��ԣ�������Ϊһ�ְ�ϸ����CD8+ Tϸ������Ҫ������ɱ������Ⱦ��ϸ��[26]�����������¶�CD8+ Tϸ�������ֿ�����ԭ����Ȼ��δ֪�ġ�
2018��1�£�Guido Silvestri�Ŷӽ�ʾ�����Ƿ��ֵ�һ�ֱ������ڰ�ü�sooty mangabey���ĺ�������������Գ������ȱ����SIV����Ⱦ��������������ڰ��̲��ļ�������ΪSIV����Ȼ�������ڰ�ü�ﲻ�Ỽ�ϰ��̲���������ԭ���ж�������������ϸ�������ϵij���ICAM2��ճ���������ڰ�ü������û�й��ܵģ�����ICAM2�����ȱʧ�ƺ������ڰ�ü���з���������SIV��������Ȼ�����������鳤�ද���������⨺����û�з������ڰ�ü���TLR4��toll������4���������ı䣬����ƻ����Ļ��ԣ����Խϵ͵�TLR4��ʽ���ܻ������SIV��Ⱦ�����������[27]�����������Ŵ��������������HIV��Ⱦ��ͨ�������鳤�ද����������ɺ��ڰ�ü�֮��Ķ�ο����ִ���SIV�������ģ������ڰ�ü�ᄀ������SIV��Ⱦ������������̲��������Ļ��ƽ������ڽ�ʾHIV�²����ơ�

ͼ12. �ڰ�ü�ͼƬ����Yerkes National Primate Research Center, Emory University��
2018��1�£�Shalley N. Kudalkar�������û��ڼ�����ͽṹ����Ʒ�����������һ�����ͻ�����������Ϊ������I��naphthyl catechol phenyl ether�����Ի�����I�������Ż�����ǿ������DZ���������䶾�����ã����Ҹ���ҩ����������[28]������Դ����С���У�������I�ܹ�����HIV��С��ѪҺ��������ˮƽ��ͬʱ���ܱ�����������ϸ�����ܸ�Ⱦ��
2018��1�£�Cheng-ting Tsai���˿�������һ�ַ�����ֿɿ���������ҺHIV������Է�����������PCR�����⣨Antibody Detection by Agglutination�CPCR, ADAP�������ַ����Ĺؼ����ڿ����һ���ؼ�����---�����������ۣ�ÿ���۶������ؽ�ϵ�HIV�����ϡ����ǻ�ȡHIV��ԭ����p24, gp41��gp120�����������ŵ�һ������DNA��ssDNA��Ƭ���ϣ��γ�HIV��ԭ-ssDNAż���������ǽ�����ż������뵽��Һ�����С����������������HIV���壬��ô���ǵ������۾ͻ�ץסHIV��ԭ-ssDNAż���Ȼ����DNA����ø���ŽӹѺ�����Ĵ����£��γ�ȫ����˫��DNAƬ�Σ���������ʵʱ����PCR����DNA�������Ӷ��Ϳɼ�������е�HIV����Ũ��[29]��
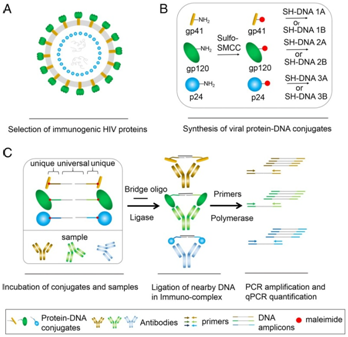
ͼ13. ����PCR������ʾ��ͼ��ͼƬ����PNAS, doi:10.1073/pnas.1711004115��
2018��1�£�R Scott McClelland�������ö������������������ռ������ݣ�����7��ϸ�����ֵ���Ũ�ȵش�����Ů�Ե�����ʱ�����ܻ������������Ǹ�Ⱦ��HIV�ķ���[30]����7��ϸ��������1�ͺ�2����������������߲�����������Gemella asaccharolytica��������֧ԭ�壨Mycoplasma hominis������ë����Leptotrichia/Sneathia����1����������Eggerthella species Type 1�����������������vaginal Megasphaera��������7��ϸ�������У���Ϊ��������1����������Parvimonas Type 1��������һ�ֳ����IJ����ر����˵��ǵ�ϸ������������Щ�о���Ա���֣���ЩЯ���Ÿ�Ũ�ȵ�1����������Ů��Ҫ����Щû��Я���Ÿ�Ũ�ȵĵ�1����������Ů���и��ߵļ��ʣ�Ϊ���ߵ�1��4.6������Ⱦ��HIV��
��ʵ����ѧ�������HIV������о���ʤö�٣��������еĽ������е�һС���֡���Ȼ�����е�һЩ�漰HIV���о���������ϸ��ģ�ͺͶ���ģ���ϣ�������Ȼ�ѿ�չ�����ٴ����飬������Ȼͣ����I�ڻ�II���ٴ�����Σ������ٴ�����Ļ���������Ȼƫ�٣�����ͨ����ļ����Ļ�����������չIII���ٴ����顣��ˣ������ܷ�õ�������ܻ�������������δ֪����������2018��Ҳ�ж���ҩ�ﱻ����������HIV��Ⱦ�����缪���¹�˾��ҩBiktarvy������FDA����������HIV-1��Ⱦ���Ƽ�������ÿ�ղ�ǰ��ͺ�ڷ�һ�Σ���ԣ��ҩ��TaiMed Biologics����Trogarzo��ibalizumab-uiyk����Ϊһ��ȫ�µĿ���ת¼�����Ʒ���FDA�������������ж����Ʒ�������Ч�ij���HIV��Ⱦ�ߣ���Ϊǰ�����������з���ȫ���һ����ЧHIV-1�ں����Ƽ����й���һ��ԭ��������ҩ����������ע���ð���Τ̩�����й�CFDA�����У���������������ѧ�������氢������Ƭ�����ݷ�������ѧ��������������Ƭ�������٣���ѧ������ƥΤ��Ƭ��������������ѧ������«��Τ����˾��Ƭ��Ҳ�Ⱥ����й����У�������˾������Symfi��Symfi Lo��Cimduo������FDA�����еȵȡ�Ψһ������ǣ���Щҩ�ﶼ������HIV��Ⱦ����δ������ѧ���ǽ��Ӳ���ѧ����������ѧ����������ѧ�Ȳ�ͬ�Ƕ�����̽��HIV��Ⱦ���ƣ����������г�һ���ܹ�����HIV��Ⱦ��������� Bioon.com��
�ο����ף�
1.EP Gelmann et al. Proviral DNA of a retrovirus, human T-cell leukemia virus, in two patients with AIDS. Science, 20 May 1983, 220(4599):862-865, doi:10.1126/science.6601822.
2.RC Gallo et al. Isolation of human T-cell leukemia virus in acquired immune deficiency syndrome (AIDS). Science, 20 May 1983, 220(4599):865-867, doi:10.1126/science.6601823.
3.F Barre-Sinoussi et al. Isolation of a T-lymphotropic retrovirus from a patient at risk for acquired immune deficiency syndrome (AIDS). Science, 20 May 1983, 220(4599):868-871, doi:10.1126/science.6189183.
4.Gero H��tter et al. Long-Term Control of HIV by CCR5 Delta32/Delta32 Stem-Cell Transplantation. NEJM, 12 February 2009, 360(7):692-698, doi:10.1056/NEJMoa0802905.
5. New UNAIDS report shows that 75% of all people living with HIV know their HIV status.
6.Benni Vargas et al. Inhibitors of Signaling Pathways that Block Reversal of HIV-1 Latency. Antimicrobial Agents and Chemotherapy, 2018, DOI: 10.1128/AAC.01744-18.
7.Joakim Esbjörnsson et al. Long-term follow-up of HIV-2-related AIDS and mortality in Guinea-Bissau: a prospective open cohort study. Lancet HIV, Published Online: 01 Nov 2018, doi:10.1016/S2352-3018(18)30254-6.
8.Linling He et al. HIV-1 vaccine design through minimizing envelope metastability, Science Advances (2018). DOI: 10.1126/sciadv.aau6769.
9.M. Uzzan el al. Anti-a4ß7 therapy targets lymphoid aggregates in the gastrointestinal tract of HIV-1�Cinfected individuals. Science Translational Medicine (2018), doi:10.1126/scitranslmed.aau4711.
10.Erica N. Borducchi et al. Antibody and TLR7 agonist delay viral rebound in SHIV-infected monkeys. Nature, Published Online: 03 October 2018, doi:10.1038/s41586-018-0600-6.
11.Mohamed Shehata Draz et al. DNA engineered micromotors powered by metal nanoparticles for motion based cellphone diagnostics. Nature Communications, Published Online: 16 October 2018, doi:10.1038/s41467-018-06727-8.
12.Pilar Mendoza et al. Combination therapy with anti-HIV-1 antibodies maintains viral suppression. Nature, 27 Sep 2018, 561(7724):479�C484, doi:10.1038/s41586-018-0531-2.
13.Yotam Bar-On et al. Safety and antiviral activity of combination HIV-1 broadly neutralizing antibodies in viremic individuals. Nature Medicine, Published Online: 26 September 2018, doi:10.1038/s41591-018-0186-4.
14.Julia A. Sung et al. HIV-Specific, Ex Vivo Expanded T Cell Therapy: Feasibility, Safety, and Efficacy in ART-Suppressed HIV-Infected Individuals. Molecular Therapy, Published Online: 21 September 2018, doi:10.1016/j.ymthe.2018.08.015.
15.Robert A. Dick, Kaneil K. Zadrozny, Chaoyi Xu et al. Inositol phosphates are assembly co-factors for HIV-1. Nature, Published Online: 01 August 2018, doi:10.1038/s41586-018-0396-4.
16.Brinda Emu et al. Phase 3 Study of Ibalizumab for Multidrug-Resistant HIV-1. New England Journal of Medicine, August 16, 2018, 379:645-654, doi:10.1056/NEJMoa1711460.
17.Dan H Barouch et al. Evaluation of a mosaic HIV-1 vaccine in a multicentre, randomised, double-blind, placebo-controlled, phase 1/2a clinical trial (APPROACH) and in rhesus monkeys (NHP 13-19). The Lancet, Published online: 06 July 2018, doi:10.1016/S0140-6736(18)31364-3.
18.Jenna B. Honeycutt et al. T cells establish and maintain CNS viral infection in HIV-infected humanized mice. Journal of Clinical Investigation, Published online:June 4, 2018, doi:10.1172/JCI98968.
19.Kai Xu et al. Epitope-based vaccine design yields fusion peptide-directed antibodies that neutralize diverse strains of HIV-1. Nature Medicine, Published online:04 June 2018, doi:10.1038/s41591-018-0042-6.
20.Lijuan Yin et al. CRISPR/Cas9 Inhibits Multiple Steps of HIV-1 Infection. Human Gene Therapy, Published Online: 9 May 2018, doi:10.1089/hum.2018.018.
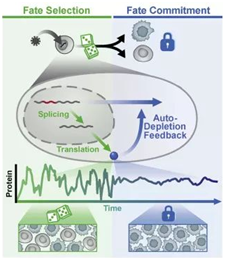
21.Maike M.K. Hansen et al. A Post-Transcriptional Feedback Mechanism for Noise Suppression and Fate Stabilization. Cell, Published online:May 10, 2018, doi:10.1016/j.cell.2018.04.005.
22.Rajeev Gautam et al. A single injection of crystallizable fragment domain�Cmodified antibodies elicits durable protection from SHIV infection, Nature Medicine (2018). DOI: 10.1038/s41591-018-0001-2.
23.Guochun Jiang et al. HIV latency is reversed by ACSS2-driven histone crotonylation. J Clin Invest. 2018 Mar 1;128(3):1190-1198. doi: 10.1172/JCI98071.
24.Ryan P. McNamara et al. Nef Secretion into Extracellular Vesicles or Exosomes Is Conserved across Human and Simian Immunodeficiency Viruses, mBio (2018). DOI: 10.1128/mBio.02344-17.
25.Xilin Wu et al. Tandem bispecific neutralizing antibody eliminates HIV-1 infection in humanized mice. Journal of Clinical Investigation (2018), doi:10.1172/JCI96764.
26.Szu-Han Huang et al. Latent HIV reservoirs exhibit inherent resistance to elimination by CD8+ T cells. Journal of Clinical Investigation, First published January 22, 2018, doi:10.1172/JCI97555.
27.David Palesch, Steven E. Bosinger, Gregory K. Tharp et al. Sooty mangabey genome sequence provides insight into AIDS resistance in a natural SIV host. Nature, 04 January 2018, 553:77�C81, doi:10.1038/nature25140.
28.Shalley N. Kudalkar et al. From in silico hit to long-acting late-stage preclinical candidate to combat HIV-1 infection. PNAS, 23 January 2018, 115(4):802-811, doi:10.1073/pnas.1717932115.
29.Cheng-ting Tsai et al. Antibody detection by agglutination�CPCR (ADAP) enables early diagnosis of HIV infection by oral fluid analysis. PNAS, Published online: January 22, 2018, doi:10.1073/pnas.1711004115.
30.R Scott McClelland et al. Evaluation of the association between the concentrations of key vaginal bacteria and the increased risk of HIV acquisition in African women from five cohorts: a nested case-control study. Lancet Infectious Diseases, Published online: 25 January 2018, doi:10.1016/S1473-3099(18)30058-6.